海纳百川和谐共进
学术分享
靶向铁自噬治疗器官损伤新策略
铁代谢紊乱是多种重大疾病的重要病理基础。铁自噬由核受体共激活因子4(NCOA4)介导,通过将储存铁的铁蛋白(ferritin)运送至溶酶体进行降解,从而释放出可利用的游离铁(Fe??)。在生理条件下,适度的铁自噬有助于维持细胞铁稳态,并支持线粒体能量代谢、DNA合成等重要生命活动。然而,当铁自噬过度激活时,细胞内游离铁迅速积累,可通过Fenton反应产生大量活性氧(ROS),诱导脂质过氧化,最终触发一种特殊的细胞死亡方式——铁死亡(ferroptosis)。
近日,天津大学海河医院陈怀永团队在期刊Autophagy发表综述论文,系统总结了铁自噬在多器官损伤中的分子机制,并提出了靶向铁自噬治疗器官损伤的新策略。

铁自噬与心脏损伤
心脏具有极高的能量代谢需求,而再生能力有限,因此对铁代谢紊乱尤为敏感。在心力衰竭、心肌缺血再灌注损伤以及脓毒症心肌病等疾病中,铁自噬常被异常激活。研究发现,NCOA4表达上调可促进铁蛋白降解并释放大量游离铁,诱导ROS爆发,从而触发心肌细胞铁死亡。在小鼠主动脉缩窄(TAC)模型中,NCOA4依赖性铁自噬明显增强,而铁死亡抑制剂Fer-1可有效减轻心肌损伤。高脂饮食还可通过IL6-STAT3信号通路上调NCOA4表达,加剧心肌细胞死亡。此外,一些常用药物也被发现能够调控铁自噬。例如黄芩苷(baicalin)和阿托伐他汀(atorvastatin)均可抑制过度铁自噬,从而改善心功能。这些研究为定量评估铁自噬在心血管疾病中的作用提供了重要证据。
铁自噬与肝脏损伤
肝脏是机体铁代谢的核心器官,因此铁自噬在多种肝病中发挥重要作用,但其功能具有“双刃剑”特征。在肝纤维化中,铁自噬可促进肝星状细胞(HSC)发生铁死亡,从而抑制纤维化进展。例如,sorafenib、curcumin和dihydroartemisinin等药物可通过激活NCOA4介导的铁自噬诱导HSC铁死亡。在肝细胞癌中,铁自噬同样可以诱导肿瘤细胞铁死亡,从而抑制肿瘤生长。一些天然产物,如caryophyllene oxide和esculetin,能够通过激活铁自噬增强抗肿瘤作用。然而,在药物性肝损伤中,铁过载则会加剧肝细胞死亡。研究表明,新型纳米材料PAA@Mn?O?可以通过抑制溶酶体中铁蛋白的降解,降低铁释放,从而缓解急性肝损伤。
铁自噬与肺脏损伤
肺组织暴露于外界环境,极易受到氧化应激损伤。近年来研究表明,铁自噬在急性呼吸窘迫综合征(ARDS)、慢性阻塞性肺疾病(COPD)、哮喘以及肺纤维化等多种肺部疾病中均发挥重要作用。在ARDS中,脂多糖(LPS)刺激或机械通气可激活AMPK-ULK1信号通路,导致NCOA4上调,从而诱导肺泡上皮细胞铁死亡。研究还发现,YAP1能够阻断NCOA4与FTH1的结合,抑制铁自噬过程。在COPD中,香烟烟雾提取物可诱导NCOA4表达,促进肺泡上皮细胞铁死亡,而沉默NCOA4则可明显减轻肺损伤。在哮喘中,IL-13刺激支气管上皮细胞上调NCOA4和TFRC表达,促进铁死亡;应用铁死亡抑制剂可缓解气道炎症反应。在肺纤维化中,dihydroartemisinin可通过激活铁自噬诱导纤维化细胞死亡,从而抑制纤维化进展;而dihydroquercetin则通过抑制铁自噬减轻硅肺纤维化,进一步表明铁自噬在不同疾病阶段可能发挥不同作用。
铁自噬与肾脏损伤
肾小管上皮细胞对铁过载高度敏感。在缺血再灌注损伤、顺铂等毒性药物损伤以及感染相关急性肾损伤中,铁自噬被显著激活。研究发现,冷诱导RNA结合蛋白(CIRBP)可上调ELAVL1表达,进而激活NCOA4依赖性铁自噬,促进铁释放并诱导肾小管上皮细胞铁死亡。一些天然化合物具有潜在保护作用。例如,silibinin可结合FTH1并阻断其与NCOA4结合;curcumin可通过激活NFE2L2抑制NCOA4表达;而SGLT2抑制剂也可能通过间接调控铁自噬改善慢性肾病预后。值得注意的是,研究还发现牛病毒性腹泻病毒感染可通过NCOA4促进线粒体铁蛋白降解,从而诱发炎症性肾损伤,提示铁自噬在感染性疾病中的潜在作用。
靶向铁自噬:器官损伤治疗的新方向
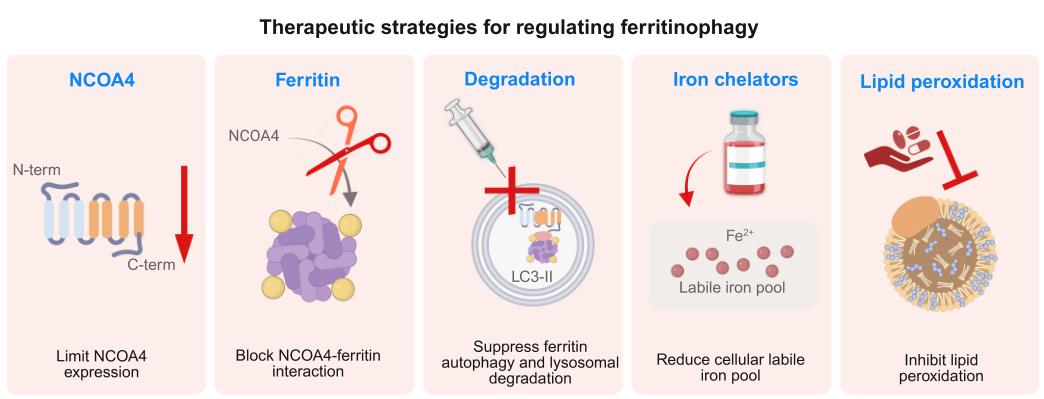
基于现有研究证据,团队提出了五类靶向铁自噬的潜在干预策略:
1.抑制NCOA4表达
2.阻断NCOA4-FTH1结合
3.抑制溶酶体介导的铁蛋白降解
4.降低细胞内游离铁水平
5.抑制脂质过氧化反应
这些策略为多器官损伤的治疗提供了新的思路。不过,研究团队也指出,目前该领域仍面临若干挑战。例如,不同器官中铁自噬调控机制存在明显差异,尚缺乏系统性比较研究;同时,仍缺少活体、实时、无创的铁自噬成像技术。此外,NCOA4除参与铁自噬外,还可能参与转录调控和DNA代谢,因此靶向NCOA4可能存在潜在脱靶风险。目前也尚无进入临床阶段的NCOA4特异性抑制剂。未来,随着单细胞测序、空间转录组学、CRISPR筛选以及PROTAC等新技术的发展,铁自噬研究有望从基础机制走向临床转化,为多种器官损伤性疾病带来新的治疗机遇。
点
点击“阅读原文”查看全文
作者介绍

论文第一作者为邵宁宁,于洪志主任为共同第一作者,陈怀永研究员为通讯作者,天津大学医学部董津睿教授为共同通讯作者,研究工作获科技部重点研发计划,国家自然科学基金,天津市自然科学基金等项目资助。

陈怀永
天津大学海河医院研究员,天津市肺脏再生医学重点实验室主任,博士生导师,长期致力于类器官、肺干细胞与肺部疾病研究。
供稿:天津市肺脏再生医学重点实验室
|


